Hukum-hukum dasar kimia adalah prinsip kuantitatif yang mengatur hubungan massa, volume, dan partikel dalam reaksi kimia, terdiri dari Hukum Lavoisier (Kekekalan Massa), Hukum Proust (Perbandingan Tetap), Hukum Dalton (Perbandingan Berganda), Hukum Gay-Lussac (Perbandingan Volume), dan Hipotesis Avogadro, yang menjadi fondasi perhitungan stoikiometri. Hukum-hukum ini menjelaskan bagaimana unsur bergabung membentuk senyawa dan bagaimana zat bereaksi dalam kuantitas yang terukur.

- Hukum Lavoisier (Hukum Kekekalan Massa): Massa total zat sebelum reaksi kimia sama dengan massa total zat setelah reaksi (massa tidak berubah).
- Hukum Proust (Hukum Perbandingan Tetap): Perbandingan massa unsur-unsur dalam suatu senyawa selalu tetap (misalnya, air selalu H:O = 1:8).
- Hukum Dalton (Hukum Perbandingan Berganda): Jika dua unsur membentuk lebih dari satu senyawa, perbandingan massa salah satu unsur akan merupakan bilangan bulat sederhana jika massa unsur lain tetap. ontohnya oksida karbon dan oksida nitrogen. Senyawa yang digunakan Dalton adalah karbon monoksida (CO) dan karbon dioksida (CO2). Dari perbandingan keduanya, diperoleh hasil sebagai berikut;

dari tabel diatas, Jika massa karbon di dalam CO dan CO2 sama, massa oksigen di dalamnya akan memenuhi perbandingan tertentu. Perbandingan massa oksigen pada senyawa CO dan CO2 yang diperoleh Dalton adalah 4 : 8 = 1 : 2
4. Hukum Gay-Lussac (Hukum Perbandingan Volume): Pada suhu dan tekanan yang sama, volume gas-gas yang bereaksi dan bervolume gas hasil reaksi berbanding sebagai bilangan bulat sederhana.
Berdasarkan penelitiannya, Lusac mengambil kesimpulan bahwa perubahan volume gas dipengaruhi oleh suhu dan tekanan. Pada suhu dan tekanan tertentu, 1 liter gas nitrogen bisa bereaksi dengan 3 liter gas hidrogen menghasilkan 2 liter gas amonia. Adapun persamaan reaksinya adalah sebagai berikut ;
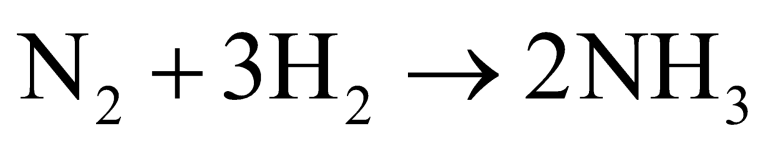
5. Hipotesis Avogadro: Pada suhu dan tekanan yang sama, gas-gas dengan volume yang sama mengandung jumlah molekul yang sama.
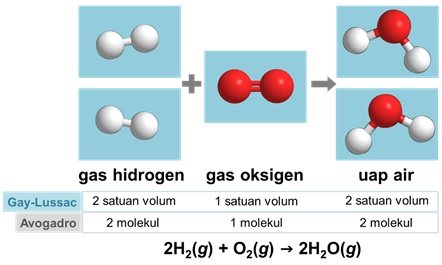
Dengan adanya hipotesis tersebut, diperoleh bahwa perbandingan volume gas sama dengan perbandingan koefisien. Secara matematis, dirumuskan sebagai berikut.
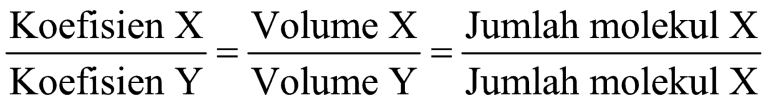
Contoh Soal
Soal 1 (Hukum Lavoisier)
Besi bermassa 21 gram direaksikan dengan belerang sehingga membentuk 33 gram besi belerang. Tentukan massa belerang yang bereaksi!
Pembahasan:
Sebelum menentukan massa belerang yang bereaksi, Quipperian bisa menulis persamaan reaksinya seperti berikut.

Hukum Lavoisier menyatakan bahwa massa zat sebelum dan setelah reaksi adalah sama, sehingga diperoleh:

Jadi, massa belerang yang bereaksi adalah 12 gram.
Contoh Soal 2 (Hukum Proust)
Dari soal tersebut diketahui:

Dengan menggunakan hukum perbandingan antara unsur dan massa yang diketahui, diperoleh:
- Massa oksigen yang diperlukan
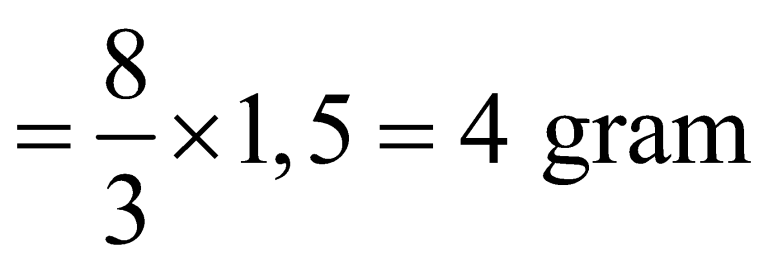
Massa karbon dioksida yang terbentuk
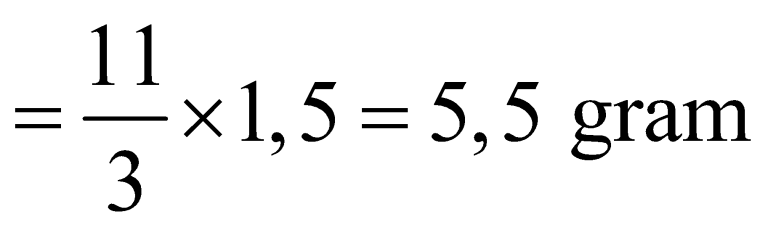
Massa karbon dioksida yang terbentuk bisa ditentukan berdasarkan persamaan hukum Lavoisier berikut.
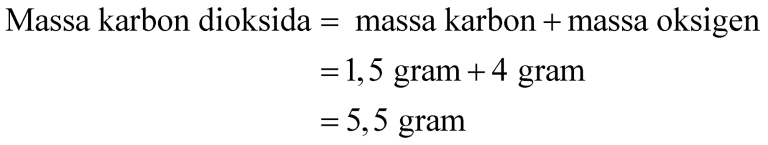
Contoh Soal 3 (Hukum Dalton)
Dua buah senyawa oksida nitrogen (NxOy) yang tersusun atas unsur oksigen dan nitrogen dengan komposisi sebagai berikut.
| Senyawa | Massa Nitrogen (gr) | Massa Oksigen (gr) |
| I | 28 | 16 |
| II | 28 | 48 |
Tentukan perbandingan antara massa oksigen pada senyawa I dan II ?
Untuk menentukan perbandingan massa oksigen pada kedua senyawa tersebut, Quipperian cukup melihat massa oksigen yang diketahui. Ternyata, cukup mudah menentukan perbandingannya ya, karena massa nitrogennya sudah sama. Secara matematis, dirumuskan sebagai berikut.
Massa oksigen I : Massa oksigen II
16 gr : 48 gr
1 : 3
Jadi, perbandingan massa oksigen pada senyawa I dan II adalah 1 : 3.
Contoh Soal 4 (Hukum Gay Lussac)
1 liter gas hidrogen bereaksi dengan 1 liter gas klorin, sehingga dihasilkan 2 liter gas hidrogen klorida. Jika gas hidrogen yang direaksikan 5 liter, tentukan gas hidrogen klorida yang dihasilkan!
Pembahasan:
Untuk menentukan volume gas hidrogen klorida yang dihasilkan, Quipperian bisa menggunakan perbandingan berikut dengan anggapan suhu dan tekanan tidak berubah.

Jadi, volume gas hidrogen klorida yang dihasilkan adalah 10 liter.
Contoh Soal 5 (avogadro)
Gas nitrogen dan gas hidrogen dapat bereaksi membentuk gas amoniak (NH3) pada keadaan tekanan dan suhu yang sama. Jika 40 molekul gas nitrogen, berapa molekul gas hidrogen yang diperlukan dan berapa molekul gas NH3 yang dihasilkan?
Jawaban:
Reaksi: N2 (g) + 3H2 (g) → 2 NH3 (g)
Perbandingan koefisien: 1:3:2
Perbandingan volume: 1 vol: 3 vol: 2 vol
Perbandingan molekul : 40 molekul: 3x 40 molekul: 2×40 molekul
Gas H2 yang diperlukan: 3×40 molekul= 120 molekul
Gas NH3 yang terjadi: 2×40 molekul= 80 molekul
Jadi, gas H2 yang diperlukan adalah 120 molekul dan NH3 yang terjadi adalah 80 molekul.
Demikianlah materi hukum Kimia, selamat belajar dan pahami serta lakukan pengulangan baik dari membaca atau melatih contoh contoh soal lainnya.