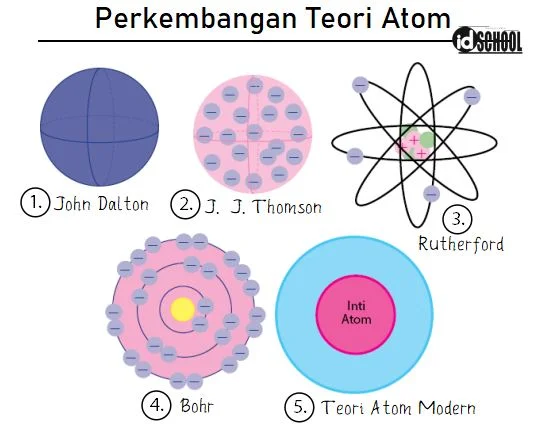
Teori atom adalah penjelasan ilmiah tentang partikel dasar materi (atom) yang berkembang dari model bola pejal Dalton, model roti kismis Thomson, model inti Rutherford, hingga model modern mekanika kuantum (orbital) yang diterima saat ini, yang menggambarkan atom terdiri dari inti (proton & neutron) dan elektron yang bergerak dalam orbital dengan tingkat energi tertentu, bukan lintasan tetap. Perkembangan ini dimulai dari ide filsuf Yunani kuno hingga penemuan partikel subatomik, membentuk dasar kimia dan fisika modern
Perkembangan Teori Atom (Model Atom)
- Teori Atom Dalton (Bola Pejal):
- Atom adalah partikel terkecil materi yang tidak dapat dibagi lagi.
- Setiap unsur memiliki atom yang identik.
- Atom bergabung membentuk senyawa dengan perbandingan tetap.
- Model Atom Thomson (Roti Kismis):
- Atom adalah bola bermuatan positif dengan elektron (negatif) tersebar di dalamnya.
- Jumlah muatan positif dan negatif sama, sehingga atom netral.
- Model Atom Rutherford (Nuklir):
- Atom memiliki inti kecil bermuatan positif (nukleus) dan elektron mengelilinginya.
- Kelemahan: Tidak bisa menjelaskan mengapa elektron tidak jatuh ke inti.
- Model Atom Bohr:
- Elektron mengorbit inti pada lintasan atau kulit-kulit tertentu dengan tingkat energi diskret (terkuantisasi).
- Elektron dapat berpindah kulit dengan menyerap atau memancarkan energi.
- Model Atom Mekanika Kuantum (Modern):
- Elektron tidak memiliki lintasan pasti, tetapi menempati orbital (daerah kebolehjadian menemukan elektron).
- Orbital memiliki bentuk dan tingkat energi tertentu (s, p, d, f).
- Didasarkan pada prinsip ketidakpastian Heisenberg dan persamaan Schrödinger.
.