
Tata nama kimia adalah sistem penamaan senyawa kimia yang terstandar, diatur oleh IUPAC, untuk memberikan nama unik yang jelas berdasarkan komposisi dan strukturnya, dibedakan menjadi tata nama anorganik (ionik, asam, basa) dan organik (senyawa karbon), menggunakan awalan angka (mono-, di-, tri-) untuk senyawa molekuler dan angka Romawi untuk kation logam dengan valensi berbeda, serta akhiran "-ida" untuk unsur kedua pada senyawa biner non-logam
1. Tata Nama Senyawa Ionik (Logam + Non-logam)
- Aturan: Nama kation (logam) + nama anion (non-logam dengan akhiran "-ida").
- Jika logam punya banyak valensi: Gunakan angka Romawi untuk menunjukkan muatannya.
- Contoh:
- NaCl: Natrium klorida.
- FeCl₂: Besi(II) klorida.
- Fe₂O₃: Besi(III) oksida.
2. Tata Nama Senyawa Molekuler (Non-logam + Non-logam)
- Aturan: Gunakan awalan angka Yunani (mono-, di-, tri-, tetra-, dll.) untuk menunjukkan jumlah atom, unsur kedua diakhiri "-ida".
- Pengecualian: Unsur pertama tidak pakai awalan "mono-" jika hanya satu atom.
- Contoh:
- CO: Karbon monoksida.
- CO₂: Karbon dioksida.
- N₂O₅: Dinitrogen pentaoksida.
3. Tata Nama Asam
- Asam Biner (H + Non-logam): "Asam" + nama non-logam dengan akhiran "-ida".
- Contoh: HCl (Asam klorida).
- Asam Oksi (H + Ion Poliatomik): "Asam" + nama anion poliatomik, akhiran berubah (misal, -at jadi -ik, -it jadi -us).
- Contoh: H₂SO₄ (Asam sulfat), HNO₃ (Asam nitrat).
4. Tata Nama Basa
- Aturan: Nama logam + "hidroksida".
- Jika logam punya banyak valensi: Tambahkan angka Romawi.
- Contoh:
- NaOH: Natrium hidroksida.
- Fe(OH)₃: Besi(III) hidroksida.
5. Ion Poliatomik Umum
- Kation: Amonium (NH₄⁺).
- Anion: Nitrat (NO₃⁻), Sulfat (SO₄²⁻), Karbonat (CO₃²⁻), Hidroksida (OH⁻), Asetat (C₂H₃O₂⁻).

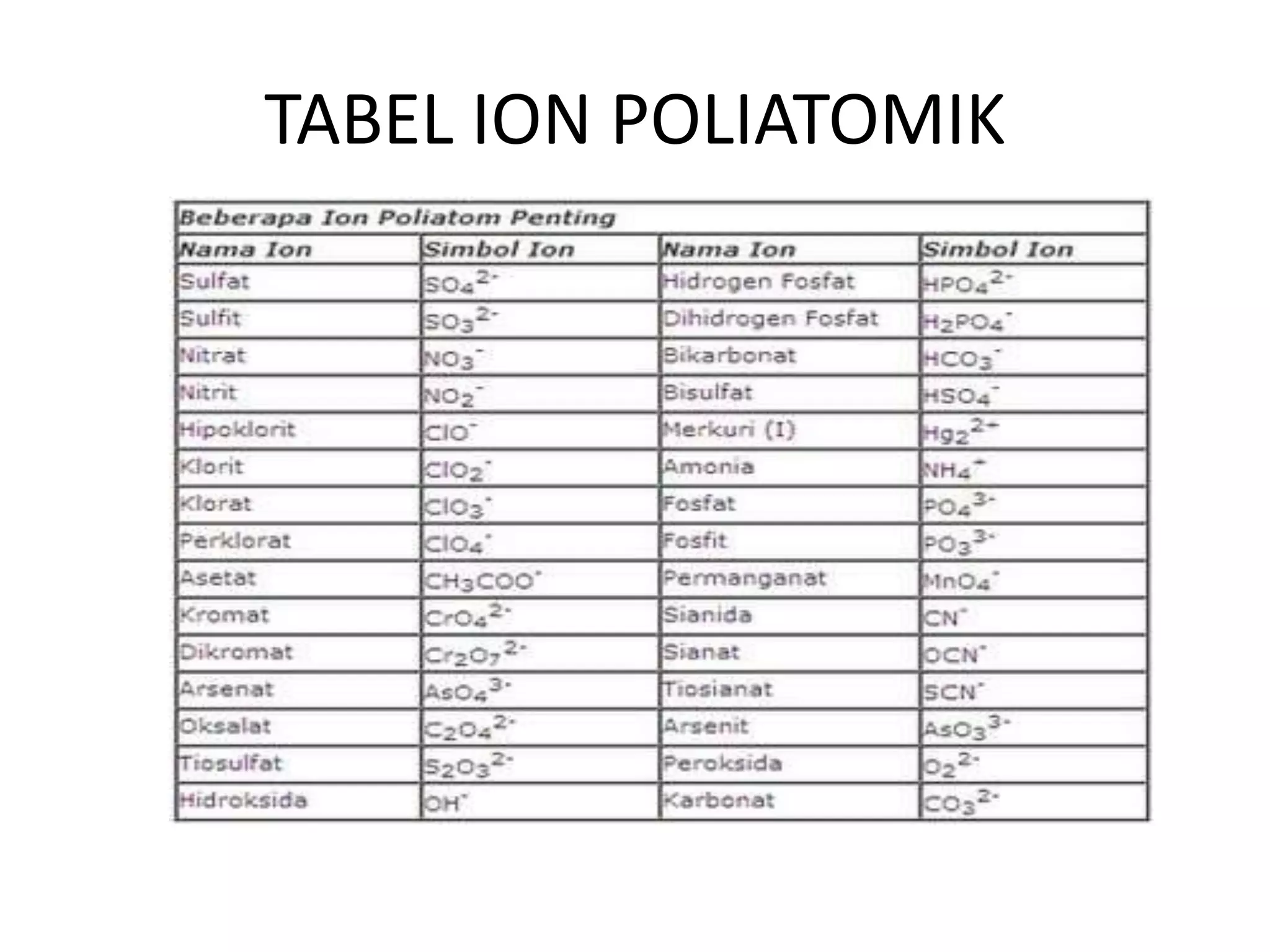
gbr2. tabel nama standar
Tata nama kimia adalah sistem penamaan senyawa kimia yang terstandar, diatur oleh IUPAC, untuk memberikan nama unik yang jelas berdasarkan komposisi dan strukturnya, dibedakan menjadi tata nama anorganik (ionik, asam, basa) dan organik (senyawa karbon), menggunakan awalan angka (mono-, di-, tri-) untuk senyawa molekuler dan angka Romawi untuk kation logam dengan valensi berbeda, serta akhiran "-ida" untuk unsur kedua pada senyawa biner non-logam
1. Tata Nama Senyawa Ionik (Logam + Non-logam)
- Aturan: Nama kation (logam) + nama anion (non-logam dengan akhiran "-ida").
- Jika logam punya banyak valensi: Gunakan angka Romawi untuk menunjukkan muatannya.
- Contoh:
- NaCl: Natrium klorida.
- FeCl₂: Besi(II) klorida.
- Fe₂O₃: Besi(III) oksida.
2. Tata Nama Senyawa Molekuler (Non-logam + Non-logam)
- Aturan: Gunakan awalan angka Yunani (mono-, di-, tri-, tetra-, dll.) untuk menunjukkan jumlah atom, unsur kedua diakhiri "-ida".
- Pengecualian: Unsur pertama tidak pakai awalan "mono-" jika hanya satu atom.
- Contoh:
- CO: Karbon monoksida.
- CO₂: Karbon dioksida.
- N₂O₅: Dinitrogen pentaoksida.
3. Tata Nama Asam
- Asam Biner (H + Non-logam): "Asam" + nama non-logam dengan akhiran "-ida".
- Contoh: HCl (Asam klorida).
- Asam Oksi (H + Ion Poliatomik): "Asam" + nama anion poliatomik, akhiran berubah (misal, -at jadi -ik, -it jadi -us).
- Contoh: H₂SO₄ (Asam sulfat), HNO₃ (Asam nitrat).
4. Tata Nama Basa
- Aturan: Nama logam + "hidroksida".
- Jika logam punya banyak valensi: Tambahkan angka Romawi.
- Contoh:
- NaOH: Natrium hidroksida.
- Fe(OH)₃: Besi(III) hidroksida.
5. Ion Poliatomik Umum
- Kation: Amonium (NH₄⁺).
- Anion: Nitrat (NO₃⁻), Sulfat (SO₄²⁻), Karbonat (CO₃²⁻), Hidroksida (OH⁻), Asetat (C₂H₃O₂⁻).






